Wiązka zadań
Nasycony roztwór nawozu sztucznego
Zadanie
Rolnik przygotował nasycony roztwór nawozu azotowego: NH4Cl (chlorku amonu), stosując wodę o temperaturze 40 °C. Część roztworu wykorzystał do przygotowania nawozu rozcieńczonego, po czym wlał do maszyny opryskującej. Niewykorzystaną resztę roztworu wstawił do ciemnej i zimnej piwnicy w zamkniętym naczyniu.
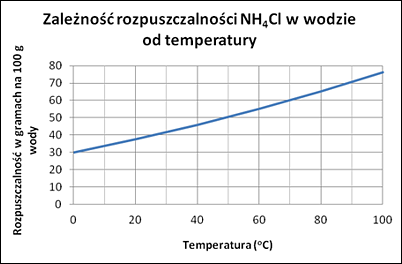
Czy po kilku dniach w naczyniu wytrącił się osad?
Przeanalizuj wykres a następnie wybierz odpowiedź i jej uzasadnienie.
Po kilku dniach w naczyniu
`square` I. wytrącił się osad / `square` II. nie wytrącił się osad
ponieważ:
`square` A. nawóz znajdował się w naczyniu zamkniętym.
`square` B. woda nie paruje z naczynia.
`square` C. w piwnicy panuje niska temperatura.
Poprawna odpowiedź
I.
C.
Wymaganie ogólne
1.1 Pozyskiwanie, przetwarzanie i tworzenie informacji. Uczeń pozyskuje i przetwarza informacje z różnorodnych źródeł z wykorzystaniem technologii informacyjno – komunikacyjnych.
2.1 Rozumowanie i zastosowanie nabytej wiedzy do rozwiązywania problemów. Uczeń opisuje właściwości substancji i wyjaśnia przebieg prostych procesów chemicznych;
2.2 Rozumowanie i zastosowanie nabytej wiedzy do rozwiązywania problemów. Uczeń zna związek właściwości różnorodnych substancji z ich zastosowaniami i ich wpływ na środowisko naturalne;
Wymaganie szczegółowe
5.4 Woda i roztwory wodne. Uczeń opisuje różnice pomiędzy roztworem rozcieńczonym, stężonym, nasyconym i nienasyconym.
5.5 Woda i roztwory wodne. Uczeń odczytuje rozpuszczalność substancji z wykresu jej rozpuszczalności.
Komentarz
Roztworom wodnym poświecony jest cały punkt 5. treści nauczania (wymagań szczegółowych), jak również dwa (8 i 9) spośród 25 doświadczeń zalecanych do przeprowadzenia na III etapie edukacyjnym w nauczaniu chemii. Podpunkt 5.3 wymagań szczegółowych podstawy programowej przedmiotu chemia stwierdza, że uczeń planuje i wykonuje doświadczenia wykazujące wpływ różnych czynników na szybkość rozpuszczania substancji stałych w wodzie. W zadaniu problem przedstawiony został w nieco inny sposób – roztwór został już przygotowany, a teraz uczeń ma za zadanie zdecydować czy i w jaki sposób wpłyną na niego warunki zewnętrzne. Tak więc podstawowym zadaniem ucznia jest skojarzenie procesu wytrącania się osadu z roztworu z warunkami w jakich znajduje się roztwór. Informację na temat zachowania się roztworu w warunkach innych niż początkowe uczniowie muszą odczytać z wykresu rozpuszczalności chlorku amonu (5.5). Zadaniem ucznia jest więc jego przeanalizowanie i stwierdzenie, że w temperaturze 40 °C rozpuszczalność tego związku wynosi około 45g na 100g wody a w temperaturze 20 °C już niecałe 40g. Trudnością dla ucznia może okazać się oszacowanie, jaka temperatura może panować w „zimnej piwnicy”. Z ogólnych informacji klimatycznych wiadomo jednak, że z pewnością poniżej 30 °C, kiedy osad NH4Cl będzie się na pewno strącać. Dodatkowo uczeń musi zauważyć, że na efekt opisany w zadaniu nie ma wpływu proces parowania, a w szczególności światło słoneczne, czy jego brak, ponieważ naczynie, w którym znajduje się roztwór jest zamknięte. Umiejętność, którą sprawdza to zadanie jest złożona – uczeń nie tylko jest zmuszony do analizy wykresu, ale również do wyciągnięcia wniosku na jego podstawie, a następnie podania jego uzasadnienia.
Utwór jest chroniony prawem autorskim. Zasady i warunki korzystania z niego określa Regulamin Serwisu Bazy Dobrych Praktyk.
"Masz uwagi do treści? Uważasz, że zawiera błąd? Napisz na bnd@ibe.edu.pl





